“El trasplante, la sustitución de un órgano destruido por otro sano, para garantizar la vida, representa la epopeya más apasionante de la ciencia médica”. Esta cita de René Küss —cirujano francés, pionero del trasplante renal y fundador de la Sociedad Francesa de Trasplante, la primera del mundo— sirve de introducción al nuevo trabajo que firman, desde la Unidad de Cirugía Experimental del Inibic y el Chuac, Marcelino González Martín —exjefe y fundador del Servicio de Urología del hospital coruñés— y Javier Rodríguez-Rivera —jefe de la Unidad Quirúrgica de Trasplante Renal del Chuac—, junto al veterinario Alberto Centeno —coordinador del Centro Tecnológico de Formación del Área Sanitaria de A Coruña y Cee—. Bajo el título Trasplante renal mirando al futuro, en el artículo trazan un mapa esperanzador del horizonte del trasplante renal, en el que el xenotrasplante —trasplante de órganos entre especies distintas— y los organoides —estructuras celulares tridimensionales capaces de reproducir las funciones de un órgano humano— jugarán un papel protagonista para hacer frente a la falta de donantes humanos.

En el mundo, explica el doctor González Martín, “se realizan cada año unos 172.000 trasplantes de órganos, según datos de la Organización Mundial de la Salud, pero la necesidad global se estima entre un millón y medio y dos millones de trasplantes anuales”. Por lo tanto, “solo se están llevando a cabo aproximadamente el 10 % de los trasplantes que se necesitarían”. Ante ese abismo entre oferta y demanda, la investigación “está muy centrada en intentar dar una solución a la gran cantidad de pacientes que necesitan un órgano, y esto pasa por el xenotrasplante y los organoides”.
Marcelino González Martín ha sido testigo y protagonista de la evolución del trasplante renal a lo largo de su carrera: fue un pionero al llevar a cabo el primero en Galicia. En 1980 su equipo realizó, en la por entonces Ciudad Sanitaria Juan Canalejo, el primer autotrasplante, un procedimiento en el que le extrajeron el riñón a una persona con estenosis arterial bilateral, reconstruyeron la arteria renal en la mesa de trabajo y se lo reimplantaron. El paciente “evolucionó sin problemas, mejorando la función del riñón autotrasplantado. Eso mostraba que el equipo estaba preparado para iniciar el programa de trasplante renal”, recuerda. Al año siguiente, en 1981, llevaron a cabo el primer homotrasplante renal de donante vivo, de padre a hijo.
Ahora, el facultativo ve esperanzas en el xenotrasplante como técnica para el corto y medio plazo. Sin embargo, no se trata de un concepto nuevo: la idea de aprovechar órganos de otras especies para salvar vidas humanas tiene más de un siglo de historia, aunque los fracasos iniciales fueron rotundos porque “no se sabía nada con respecto al rechazo”. En la década de los años sesenta, con conocimientos inmunológicos más avanzados, los cirujanos Reemtsma y Starzl utilizaron riñones de chimpancé y babuino en pacientes con insuficiencia renal, logrando supervivencias de varios días e incluso, en algún caso, de nueve meses. Pero fue el inglés Roy Calne quien, en 1970, estableció la distinción fundamental entre xenotrasplantes concordantes —aquellos entre especies filogenéticamente próximas, donde el rechazo tarda horas o días en producirse— y discordantes, donde la distancia genética provoca un rechazo hiperagudo, fulminante, que destruye el órgano trasplantado en cuestión de minutos por trombosis.
La lógica biológica señalaba a los primates no humanos como la fuente más natural de órganos para las personas, porque compartimos con el chimpancé, el orangután o el bonobo entre el 96 y el 99 % de nuestro ADN. Sin embargo, su utilización como donantes presenta grandes obstáculos. «Los primates se reproducen con dificultad en cautividad, son muy caros de mantener y su número está disminuyendo drásticamente», explica el doctor González Martín. “En 1960 había tres millones de chimpancés en el mundo, pero hoy quedan apenas 130.000”. A ello se suman “el riesgo de transmisión de enfermedades como SIDA, hepatitis, ébola o viruela” y la “inaceptabilidad ética de usar como fuente de órganos a animales tan próximos a nuestra propia especie”. El cerdo emergió entonces como la alternativa más prometedora. «Éticamente, si los utilizamos para comer, no está mal visto que los utilicemos para vivir», razona el urólogo. “Sus órganos son anatómica y fisiológicamente muy similares a los humanos —ya empleamos sus válvulas cardíacas y su insulina con fines terapéuticos—, y se reproducen en cautividad con facilidad y bajo coste”. El gran obstáculo era el rechazo hiperagudo, inevitable entre dos especies tan distantes, pero en los últimos años el avance científico ha permitido mitigar este problema.
A principios del año 2000, el equipo del doctor González Martín puso en marcha en el Chuac uno de los programas de xenotrasplante experimental más avanzados de España, financiado por la Fundación Barrié de la Maza. El proyecto consistía en realizar trasplantes de riñón de cerdo transgénico —al que se le había suprimido el antígeno galactosa-alfa-1,3-galactosa— a babuino. Entre 2000 y 2003, el equipo coruñés llevó a cabo un total de veinte xenotrasplantes. Los resultados fueron notables: en ningún caso se produjo el temido rechazo hiperagudo inmediato, y la duración media de los riñones trasplantados fue de una semana. En el mejor de los casos, el babuino receptor llegó a vivir un mes entero con el riñón porcino funcionando. «A nivel experimental fuimos los primeros en España«, explica.
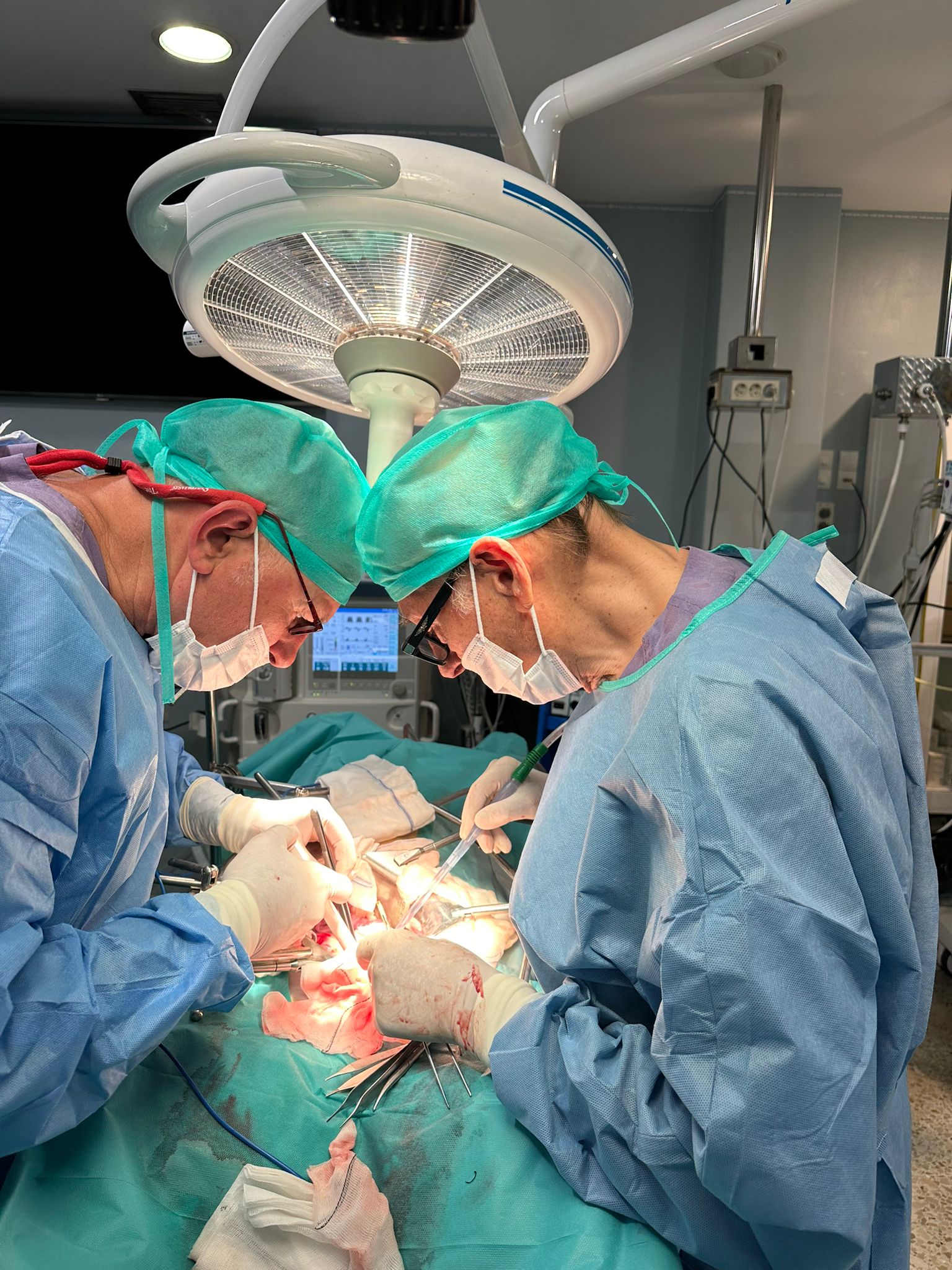
Aquella experiencia demostró que el rechazo hiperagudo podía ser controlado, al menos en parte. Pero para dar el salto al ser humano era necesario ir mucho más lejos, y la solución llegó desde los laboratorios de genómica. La irrupción de la tecnología CRISPR-Cas9 —las «tijeras genéticas» cuyo desarrollo valió el Premio Nobel de Química en 2020 a Emmanuelle Charpentier y Jennifer Doudna— abrió nuevas posibilidades. Con esta herramienta de edición genética es posible crear cerdos a medida: animales “a los que se les han eliminado unos genes para que no produzcan rechazo hiperagudo y se les han puesto otros para que se parezcan más al humano y generen menos problemas de rechazo. Con estos órganos modificados ya se ha conseguido que babuinos receptores sobrevivan hasta dos años”.
El salto a los seres humanos se produjo en 2021. Los primeros ensayos, en Estados Unidos, se realizaron en pacientes en muerte cerebral —mantenidos con latido cardíaco— con el consentimiento previo de sus familias. Se trataba de un modelo preclínico de uso compasivo que permitía obtener datos de fisiología humana sin los riesgos de un ensayo clínico convencional. La primera experiencia “duró 54 horas y confirmó que el riñón porcino transgénico funcionaba correctamente y producía orina en un cuerpo humano sin rechazo hiperagudo”. La segunda se realizó “retirando ambos riñones del cadáver y trasplantándole dos riñones de cerdo transgénicos, con resultados positivos durante 77 horas y sin rechazo hiperagudo”. En el tercer ensayo, “el paciente mantuvo el riñón funcionando durante 61 días”. En 2024, China realizó trasplantes similares de hígado y pulmón de origen porcino.
Posteriormente se ha pasado al xenotrasplante en pacientes vivos, con dos experiencias en el Hospital General de Massachusetts. El paciente del primer ensayo “falleció a los dos meses por causas ajenas al procedimiento, con el riñón funcionando perfectamente”, explica Marcelino González Martín. En enero de 2025 se realizó otro, “y hasta final de año el riñón seguía funcionando y el paciente estaba en su casa”. En Estados Unidos “ya se ha autorizado una experiencia clínica amplia en humanos con pacientes que están en lista de espera para recibir un trasplante”. Allí, “más de una docena de personas en lista de espera para trasplante de riñón mueren diariamente, por lo que, muy probablemente, los que llevan mucho tiempo esperando aceptarán el xenotrasplante».
En España, el Hospital Clínico Universitario Virgen de la Arrixaca de Murcia ha propuesto a la Organización Nacional de Trasplantes iniciar un ensayo clínico de xenotrasplante hepático porcino como órgano puente, aunque la autorización todavía está pendiente.
Por su parte, el doctor Javier Rodríguez-Rivera explica que, “actualmente, para aumentar el número de órganos ya estamos utilizando riñones de donantes subóptimos —por ejemplo, de mayor edad— o en asistolia, potenciando el trasplante renal de donante vivo y poniendo en marcha programas nacionales de intercambio de riñones, como el Plan Nacional de Acceso al Trasplante Renal para Pacientes Hiperinmunizados (PATHI)”. Como esto no es suficiente, “una de las alternativas para aumentar el número de órganos es el xenotrasplante —un futuro a cortísimo plazo—, y otra son los organoides —que representan un futuro a medio plazo, porque se encuentran en fase preclínica—”.
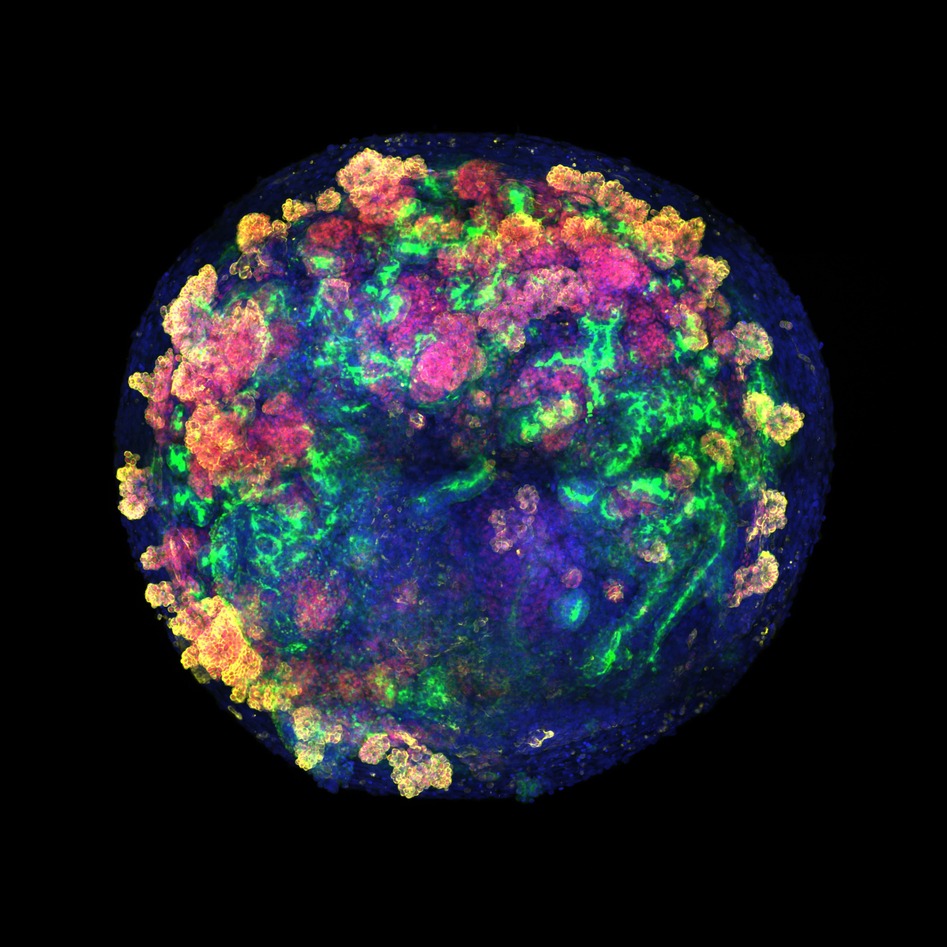
Los organoides son “estructuras celulares tridimensionales, creadas a partir de células madre en una placa de cultivo, que reproducen en miniatura la arquitectura y parte de las funciones de un órgano real”. Bajo estímulos bioquímicos externos, unas células madre pluripotenciales se transforman en células especializadas —como nefronas, en el caso del riñón—. Además, “tienen la capacidad de organizarse y diferenciarse para crear miniórganos en el laboratorio, cuya función principal es crear o producir nuevas células para reemplazar a otras que se pierden por envejecimiento del órgano”. De esta forma, “pueden servir de base para el desarrollo, en el laboratorio, de tejidos y órganos trasplantables —como ‘minirriñones’— sin riesgo de rechazo”.
En esa línea, Javier Rodríguez-Rivera ha participado en un estudio dirigido por la bióloga barcelonesa Nuria Montserrat, del Instituto de Bioingeniería de Cataluña (IBEC) y actual consejera de Investigación y Universidades de la Generalitat de Cataluña, en el que también han colaborado el Instituto de Salud Carlos III y la Organización Nacional de Trasplantes. Después de más de diez años de trabajo e investigación, el artículo ha sido publicado recientemente en la revista Nature Biomedical Engineering y recoge “una tecnología pionera que permite producir a gran escala organoides renales humanos mediante la combinación con riñones de cerdo ex vivo, que luego son trasplantados al mismo animal para evaluar su viabilidad”.
El proceso comenzó con la creación, en el IBEC, de organoides humanos—del tamaño de una cabeza de alfiler, pero con los elementos funcionales esenciales de un riñón humano— en grandes cantidades, de alta calidad y a un precio aceptable. A continuación, para validar que esos organoides podían sobrevivir e implantarse en el interior de un órgano vivo, se eligió la Unidad de Cirugía Experimental del Inibic. «Para nosotros fue un honor y una muestra de confianza enorme que un proyecto de investigación tan importante como este contara con nosotros», explica el doctor Rodríguez-Rivera. Esa confianza no fue fruto del azar: “en la unidad —que cuenta con financiación de la Fundación Amancio Ortega—, ya habíamos realizado previamente varios procedimientos quirúrgicos de autotrasplante con perfusión normotérmica en cerdos para validar la máquina de perfusión que se iba a emplear en el proyecto.
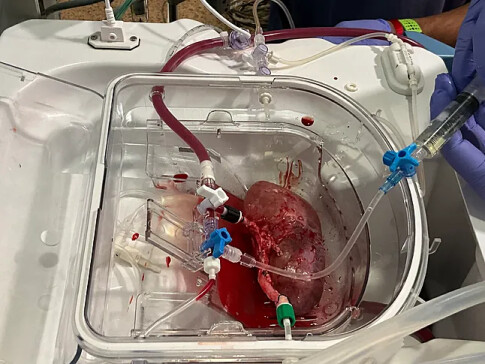
El procedimiento experimental en el Inibic se realizó con nueve cerdos. A cada uno “se le extrajo el riñón izquierdo por laparoscopia que, después, se lavó para eliminar la sangre de su sistema vascular y se colocó en una máquina de perfusión normotérmica” para mantener el órgano vivo y funcional fuera del cuerpo, perfundiendo sangre del propio cerdo y conectada a un oxigenador. En esas condiciones, los riñones se perfundían durante una hora, tras la cual se sembraban con los organoides humanos y se mantenía la perfusión otras tres horas. Las dosis variaron según el animal —sin organoides en dos cerdos de control, a dosis baja en tres, a dosis alta en uno y con células procedentes de disociación enzimática de organoides en otros dos—. Tras esas cuatro horas, “el riñón se trasplantaba de nuevo en el cerdo según técnica similar a la que se realiza en los humanos”. Los animales se sacrificaban a las 24 o 48 horas, y los riñones se analizaban en detalle mediante distintas técnicas de inmunofluorescencia, histológicas y bioquímicas”.
Los resultados demostraron tres cuestiones fundamentales: “que los organoides se asentaban en la corteza del riñón, que persistían durante 24 o 48 horas tras el trasplante y que, siendo organoides humanos, no desencadenaban respuesta inmunológica importante en el cerdo. El riñón trasplantado continuaba funcionando con normalidad y no se detectaron signos de daño ni toxicidad”. Todo ello “constituye un paso de gigante para avanzar a la siguiente fase”, asegura Javier Rodríguez-Rivera.
Ese próximo paso ya está diseñado. En coordinación con la ONT, que ha perfilado los hospitales participantes, el equipo del Inibic recibirá riñones humanos procedentes de donantes cadáver que habrían sido descartados por no cumplir las condiciones óptimas para el trasplante —algo que sucede con un millar de estos órganos cada año en España—. En estos riñones se infundirán los organoides para comprobar si los resultados observados en el modelo porcino se reproducen en tejido humano. «Ya está perfilado qué hospitales van a generar esos órganos, y nosotros vamos a encargarnos de infundir los organoides para comprobar si asientan en esos riñones humanos y no producen rechazo inmunológico. Seremos el centro que pilote la parte más importante del estudio», explica el responsable de la Unidad Quirúrgica de Trasplante Renal del Chuac.
Las implicaciones clínicas de esta línea de investigación tienen una doble vertiente. Por un lado, “mejorar riñones extraídos que no eran óptimos para el trasplante y que, al infundirles los organoides generarían más tejido nefrológico que ayudaría al paciente a recuperar la función de ese riñón. Sin ellos, los órganos se hubieran descartado”. Por otro, “poder infundir directamente organoides renales en los riñones de pacientes en severa insuficiencia renal para que regeneren tejido en sus propios riñones enfermos y eviten así un trasplante o tener que someterse a diálisis”.
La epopeya del trasplante, como la calificó Küss, sigue viva y avanza con nuevas técnicas, como el xenotrasplante y los organoides, que dibujan un futuro en el que la falta de órganos de donantes humanos no sea un obstáculo para la supervivencia. Como hace casi cincuenta años, cuando Marcelino González Martín llevaba a cabo el primer trasplante realizado en Galicia, los profesionales de nuestra provincia continúan a la vanguardia y escribiendo las páginas del futuro de la medicina.